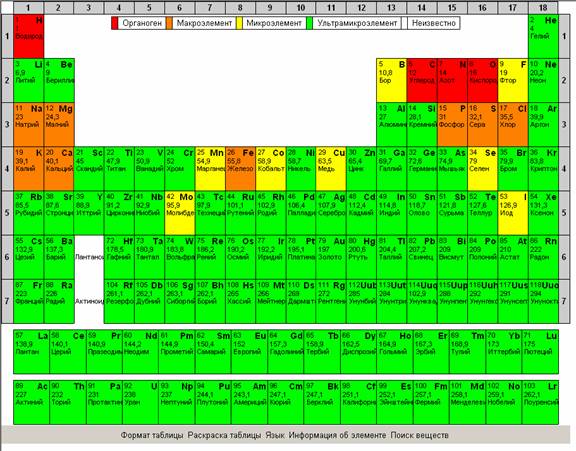
Периодический закон и Периодическая система химических элементов Д. И. Менделеева. В 1.
Д. И. Менделеев сформулировал Периодический закон следующим образом: . Позднее установлено, что порядковый номер совпадает с зарядом ядра, числом протонов в ядре и числом электронов в электронной оболочке. Периодом называется горизонтальный ряд элементов, в пределах которого свойства элементов и их соединений изменяются последовательно от металлических (основных) через амфотерные к неметаллическим (кислотным). Современная ПСХЭ состоит из семи периодов (1- 3 периоды малые, 4- 7 периоды большие). Каждый период начинается щелочным металлом и заканчивается галогеном и далее элементом, относящимся к инертным газам. При переходе к каждому следующему периоду наблюдается повторяемость свойств элементов предыдущего периода. Номер периода, в котором находится химический элемент, совпадает с числом энергетических уровней в оболочке его атома.
Номер периода в Периодической системе определяется: А). На основании положения в Периодической системе расположите элементы: Германий, Мышьяк, Сера, Фосфор – в порядке убывания окислительныхсвойств.
Каждый период начинается щелочным металлом и заканчивается галогеном и далее элементом, относящимся к инертным газам. Периодический закон и Периодическая система химиче. Тренировочный тест по теме 'Периодический закон и. Представленный тест по темам: «Строение атома. Периодический закон и Периодическая система химических элементов Д.И. Скачать: Тесты по химии. Периодический закон и периодическая система. К учебнику Рудзитиса Г.Е., Фельдмана Ф.Г. Периодический закон и периодическая система элементов Д.И. Менделеева» по предмету Химия. Категория: Печатные тесты по .
2(Б), 16(П) Периодический закон и Периодическая система химических элементов Д.И.Менделеева. Проверочный тест по теме: Соли. 6(Б) Химическая реакция. Условия и признаки протекания химических реакций. 10.(6 баллов) Как и почему в Периодической системе изменяются неметаллические свойства? В пределах главной подгруппы.
Группой называется вертикальный столбец элементов, проявляющих определённое химическое сходство. Каждая из 8 групп подразделяется на главную (а) и побочную (б) подгруппу. Номер группы, в которой находится химический элемент главной подгруппы, совпадает с числом электронов на внешнем энергетическом уровне его атома, а также показывает высшую валентность элемента и высшую степень окисления элемента в соединениях (исключения - азот и кислород). Главные подгруппы могут содержать и металлы и неметаллы. Побочные подгруппы содержат только элементы- металлы. Все элементы по способу завершения внешнего уровня при образовании химических связей делятся на металлы и неметаллы. Атомы элементов- металлов при образовании химической связи отдают электроны с внешнего (иногда и предыдущего) энергетического уровня и превращаются в катионы (положительные ионы).
Тест по химии на тему "Элементы Периодической системы химических элементов В периодической системе Менделеева сегодня 117 элементов.

Атомы элементов- неметаллов при образовании химических связей принимают недостающее до 8число электронов на внешний энергетический уровень и превращаются в анионы (отрицательные ионы). На сегодняшний день известно 2. В ПСХЭ элементы- металлы находятся слева от диагонали бор - астат и справа от диагонали только в побочных подгруппах. Элементы- неметаллы находятся справа от диагонали бор - астат в главных подгруппах и на диагонали (бор, кремний, мышьяк, теллур, астат). Атомы металлов имеют больший радиус атома и меньшее число электронов на внешнем энергетическом уровне по сравнению с атомами неметаллов. Радиус атома увеличивается в группе сверху вниз.
Радиус атома уменьшается в периоде слева направо. Число энергетических уровней у атомов элементов одного периода одинаковое (равно номеру периода). Число электронов на внешнем энергетическом уровне у атомов элементов одной группы одинаковое (равно номеру группы). Металлические свойства простых веществ, а также основные свойства оксидов и гидроксидов усиливаются в группе сверху вниз и уменьшаются в периоде слева направо.
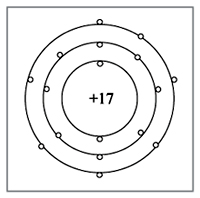
Неметаллические свойства простых веществ, а также кислотные свойства оксидов и гидроксидов усиливаются в периоде слева направо и уменьшаются в группе сверху вниз. Электроотрицательность (способность атомов элементов- неметаллов притягивать к себе общие электронные пары при образовании ковалентной полярной связи) увеличивается в периоде слева направо и в группе снизу вверх.


 RSS Feed
RSS Feed
